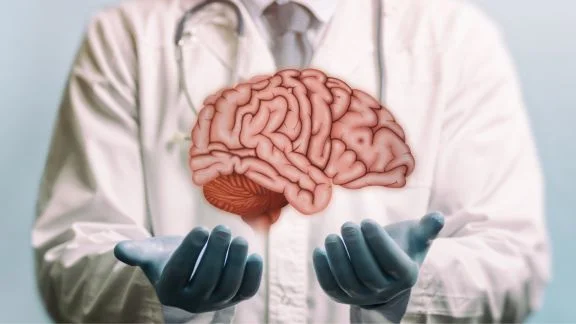
Come riconoscere l'ictus? Ischemico o emorragico: scopri le cause, i fattori di rischio e i sintomi. Cure e guarigione: terapie possibili e complicanze.

Più Selenio e meno cancro alla prostata
![]() Dr. Giovanni Beretta
Dr. Giovanni Beretta
05.12.2025 - Un’ampia meta-analisi mostra che livelli più alti di selenio riducono l’11% il rischio di tumore della prostata. Scopri risultati, dosaggi efficaci e implicazioni cliniche.

Avvicinare il medico e il paziente abbattendo le barriere socio culturali.

Aumentare la consapevolezza rispetto alle scelte sulla propria salute.

Promuovere la cultura medica per evitare l'autodiagnosi e l'autocura.
Oltre 497.1k utenti registrati si fidano di noi.
Gli Specialisti della Community, verificati alla registrazione, collaborano gratuitamente per offrire contenuti medico-scientifici accurati, veritieri e aggiornati.
I Referenti Scientifici, garanti delle Linee Guida, vigilano quotidianamente sulla qualità dei contenuti pubblicati.

Dr.ssa Mariateresa Di Taranto Psicologo

Dr. Paolo Piana Urologo

Dr. Silvio Boer Ortopedico

Dr. Domenico Spinoso Medico del lavoro

Dr.ssa Anna Potenza Psicologo

Dr. Michele Loia Psicologo

Dr.ssa Franca Scapellato Psichiatra

Dr. Salvo Catania Oncologo
Oggi già 62 risposte dai nostri medici specialisti!
Consulta l'archivio
Tra più di 1.6 milioni di consulti trova la situazione simile alla tua.
Hai un disturbo di salute?
Descrivi il tuo problema e chiedi un consulto ai nostri specialisti.
Sei uno specialista?
Aiuta gli utenti in difficoltà e rispondi ai loro dubbi.

Come riconoscere l'ictus? Ischemico o emorragico: scopri le cause, i fattori di rischio e i sintomi. Cure e guarigione: terapie possibili e complicanze.
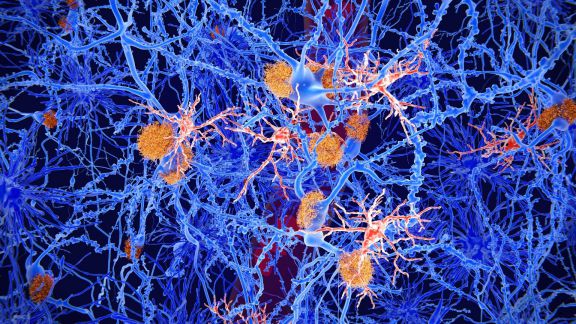
Gliosi ed esiti gliotici: quando preoccuparsi?
Dr. Ferraloro
La contraccezione con l’anello vaginale
Dr.ssa Pontello

FSH alto e 17 beta-estradiolo basso: sono in menopausa?
Dr.ssa De Falco

Le fratture del piatto tibiale
Dr. Preite
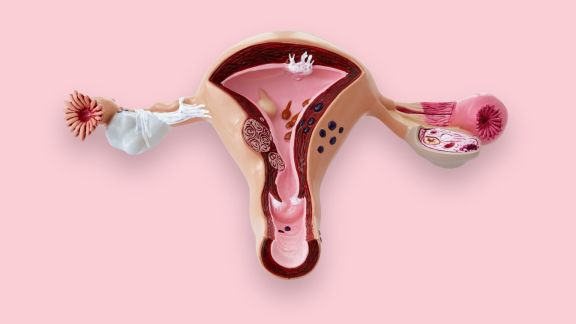
Ectopia o ectropion? Le piaghette sul collo dell'utero
Dr.ssa De Falco

Come calcolare le settimane di gravidanza?
Dr.ssa Pontello

Come si calcola
il rischio reale di tumore al seno
Storie di ragazze fuori di seno
Il primo blog di Medicina Narrativa
2.971 utenti che hanno scritto 827.872 commenti, 55.191 pagine di contenuti equivalenti nel cartaceo a 1496 volumi da 225 pagine, con oltre 600.000 visualizzazioni mensili e 36.359.849 visualizzazioni totali
Vorrei sottopormi a un consulto oculistico preventivo per verificare la mia idoneità visiva ai fini della visita militare. Attualmente porto occhiali con la seguente gradazione: Occhio destro...
Buonasera, Più di un mese fa ho avuto forte tosse con malessere generale e un solo giorno di febbre. Dopo 2 settimane forte raffreddore. Non riuscivo a scaricare, voce nasale e sensazione di...
Buonasera Dottori, Da circa un paio di mesi avverto specie di sera del prurito in tutto il corpo senza arrossamenti né punture di insetti. Non è un vero prurito da grattare ma quasi un...
Buongiorno Sono un uomo di 37 anni. All’età di 26 anni ho avuto il primo episodio di attacco di panico e ansia acuta, trattato immediatamente con escitalopram (Entact) 20 mg e gocce di Xanax. ...